- Laboratorio
- Medicina di laboratorio
- Software di gestione dati
- Charles River Laboratories
Software di analisi di dati EndoScan-V™di analisi di campionidi gestione datidi controllo

Aggiungi ai preferiti
Confronta con altri prodotti
Caratteristiche
- Funzione
- di analisi di dati, di analisi di campioni, di gestione dati, di controllo, per reportistica, di prova, di registrazione dati, di condivisione, con sistema di tracciatura, di archiviazione, di fabbricazione
- Applicazioni
- medico, per ospedale, da laboratorio, per lettore di micropiastre, per automazione di laboratorio, per l'industria farmaceutica, per farmacia, per microbiologia, per chemioterapia
- Tipo
- in tempo reale
Descrizione
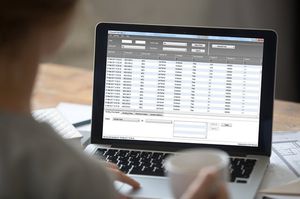
Mantenere la sicurezza a lungo termine di un ambiente di produzione, soddisfacendo al contempo le esigenze di conformità, è la priorità assoluta di un responsabile del controllo qualità microbico. Endosafe® EndoScan-V™ è il nostro software fondamentale e sicuro per la misurazione e l'analisi delle endotossine, che consente di generare e riportare i dati quantitativi dei test LAL e rCR.
Fiducia nei vostri dati
Con il crescente volume di test LAL quantitativi che vengono eseguiti ogni giorno, la generazione di dati elettronici e la conservazione sicura sono ormai un requisito, piuttosto che un'opzione. Le lettere di avvertimento della FDA e i documenti guida globali stanno aumentando i requisiti di integrità dei dati, rendendo visibili le lacune e le carenze nei dati e nelle pratiche di reporting in tutti i settori. Il software EndoScan-V per il test e l'analisi delle endotossine consente di prendere decisioni informate e sicure sulla qualità dei prodotti grazie a un'infrastruttura di gestione dei dati integrata e completa.
Le decisioni basate sui dati sono l'unico modo per confermare con sicurezza la qualità dei prodotti e garantire la sicurezza dei pazienti. Il vostro programma e la vostra piattaforma di rilevamento delle endotossine richiedono un software di analisi delle endotossine che generi un'analisi accurata dei dati grezzi per il reporting, il monitoraggio e l'andamento dei test BET, sia che si utilizzino reagenti LAL che rCR.
Maggiore coerenza e affidabilità
l'accesso a dati BET accurati e pertinenti in una piattaforma semplice e organizzata è essenziale per prendere decisioni sicure e basate sui dati. EndoScan-V è dotato di un'interfaccia intuitiva per l'accessibilità e di un backup sicuro che protegge i record storici per sbloccare la visibilità in tempo reale delle tendenze emergenti nei risultati.
---
VIDEO
Cataloghi
Altri prodotti Charles River Laboratories
Bacterial Endotoxin Testing
Ricerche correlate
- Kit di reagenti
- Kit di test
- Kit di reagenti in soluzione
- Kit di reagenti liquido
- Kit di test immunologico
- Kit di reagenti da laboratorio
- Kit di test per malattie infettive
- Software di analisi
- Kit di reagenti enzima
- Kit di reagenti soluzione tampone
- Software di controllo
- Kit ELISA
- Software da laboratorio
- Kit di reagenti batteriologico
- Software per reportistica
- Kit di test d'IgG
- Kit di test di cellule
- Software di monitoraggio
- Software automatizzato
- Software ospedaliero
* I prezzi non includono tasse, spese di consegna, dazi doganali, né eventuali costi d'installazione o di attivazione. I prezzi vengono proposti a titolo indicativo e possono subire modifiche in base al Paese, al prezzo stesso delle materie prime e al tasso di cambio.