Reagente IgG MO22196per western blotper immunofluorescenzaper immuncitochimica
Aggiungi ai preferiti
Confronta con altri prodotti
Caratteristiche
- Tipo
- IgG
- Applicazioni
- per western blot, per immunofluorescenza, per immuncitochimica
- Formato
- liquido
- Marcatore testato
- PEA15
- Origine
- estratto dal topo
- Temperatura di stoccaggio
Max.: 4 °C
(39 °F)Min.: -20 °C
(-4 °F)
Descrizione
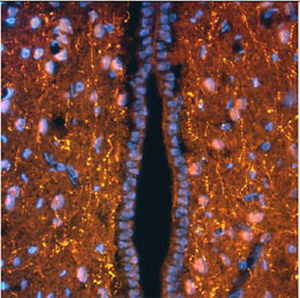
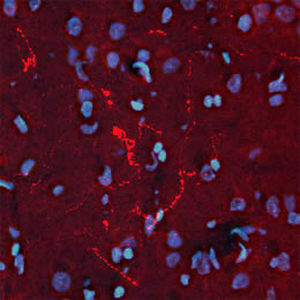
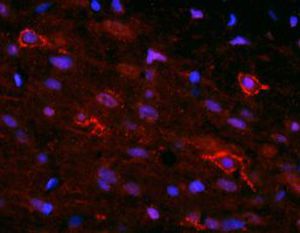
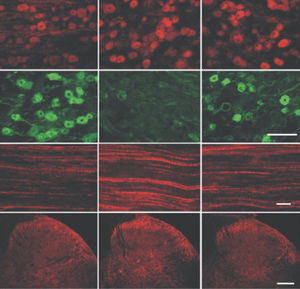
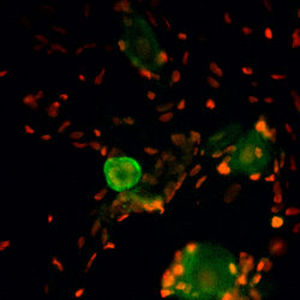
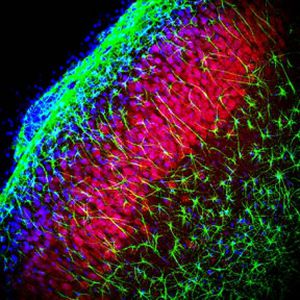
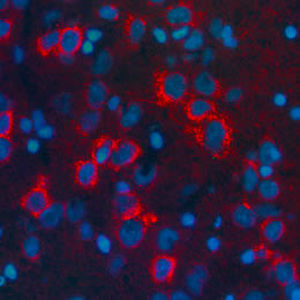
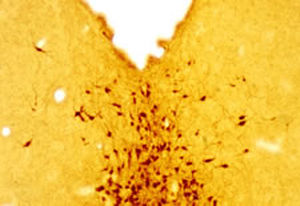
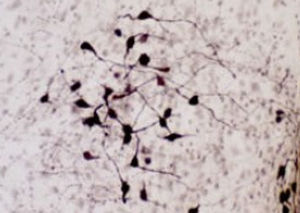
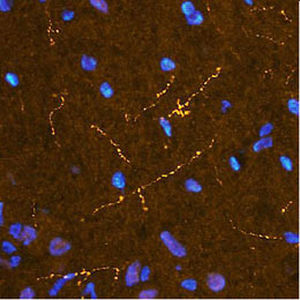
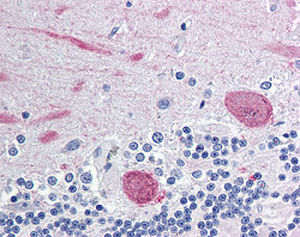
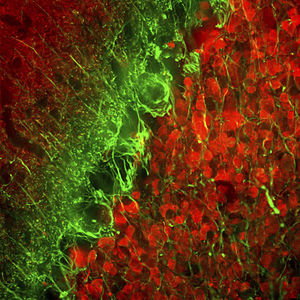
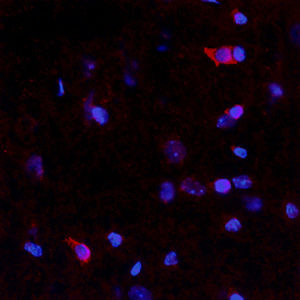
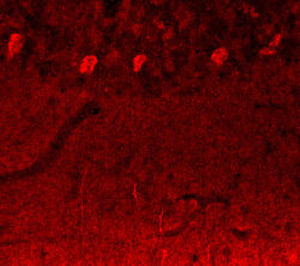
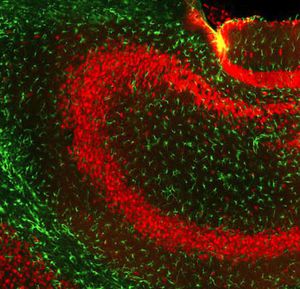
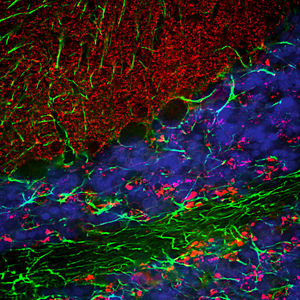
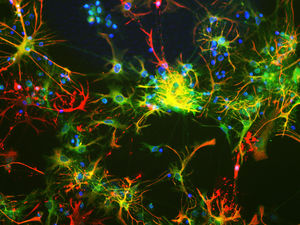
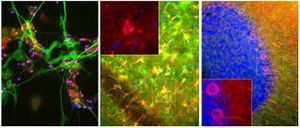
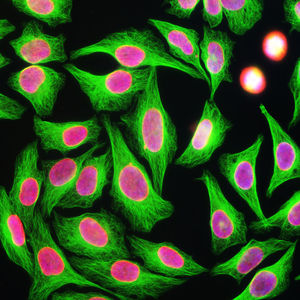
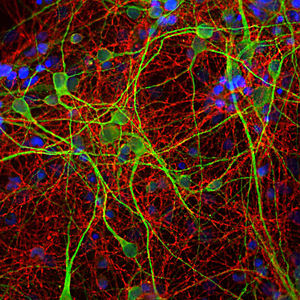
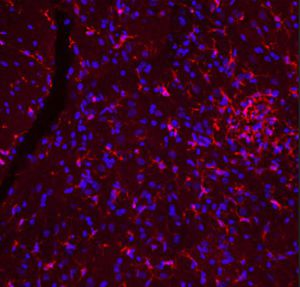
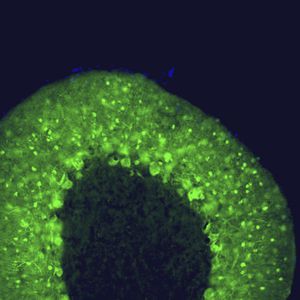
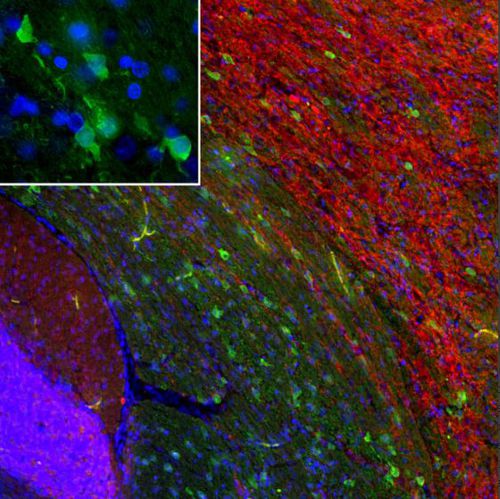
La PEA-15 è stata originariamente isolata come proteina principale a basso peso molecolare degli astrociti striatali embrionali di topo cresciuti in coltura cellulare. Tre macchie su gel 2D con un peso molecolare apparente di 15kDa e punto isoelettrico 5,1-5,3 hanno dimostrato di essere forme diverse di un'unica proteina. La proteina è stata fosforilata in serina su un sito dalla protein chinasi C sia in vivo che in vitro e la proteina è stata denominata "fosfoproteina arricchita in astrociti di 15kDa", da cui PEA-15. Il successivo clonaggio e sequenziamento ha rivelato una proteina ben conservata in sequenza tra il topo e l'uomo e fortemente espressa nel cervello. Indipendentemente, la stessa proteina è risultata up-regolata nei fibroblasti e nei tessuti di pazienti diabetici ed è stata quindi denominata "proteina arricchita nel diabete" o PED. Studi immunocitochimici hanno dimostrato che la proteina è fortemente espressa negli astrociti e in alcuni neuroni del sistema nervoso centrale dei topi, sebbene sia espressa a livelli inferiori in modo ubiquitario. È stato dimostrato che la PEA-15 interagisce con la chinasi regolata dal segnale extracellulare e regola l'ingresso nucleare di questa proteina; sono state inoltre descritte numerose altre importanti interazioni con altre proteine coinvolte nella regolazione dell'apoptosi, del metabolismo del glucosio e della crescita cellulare. MCA-4D2 è stato prodotto contro un costrutto ricombinante di PEA-15 a lunghezza intera espresso e purificato da E. coli.
---
Cataloghi
Nessun catalogo è disponibile per questo prodotto.
Vedi tutti i cataloghi di NeuromicsAltri prodotti Neuromics
Primary Antibodies
Ricerche correlate
- Kit di reagenti
- Kit di reagenti per biologia molecolare
- Kit di reagenti liquido
- Kit di reagenti da ricerca
- Kit di reagenti di proteine
- Reagente per immunologia
- Kit di reagenti anticorpo
- Kit di reagenti liofilizzato
- Kit di reagenti di siero
- Kit di reagenti per immunoistochimica
- Kit di reagenti anticorpo monoclonale
- Kit di reagenti per ricerca scientifica
- Kit di reagenti per western blot
- Kit di reagenti per immunofluorescenza
- Reagente estratto dal topo
- Reagente anticorpo policlonale
- Kit di reagenti citochina
- Kit di reagenti fattore di crescita
- Reagente IgG
- Reagente per immuncitochimica
* I prezzi non includono tasse, spese di consegna, dazi doganali, né eventuali costi d'installazione o di attivazione. I prezzi vengono proposti a titolo indicativo e possono subire modifiche in base al Paese, al prezzo stesso delle materie prime e al tasso di cambio.